E-book Doenças do Silicone 7ª Edição 2026 - Estudo Científico
Dr. Ricardo Miranda
Cirurgião plástico com atuação em São Paulo nas cirurgias das mamas e da face
CRM-SP 113.041
Cirurgião plástico
Membro titular da Sociedade Brasileira de Cirurgia Plástica Especialização em reconstrução mamária pelo Hospital Pérola Byington Fellowship em cirurgia plástica estética pela Universidade de Toronto, Canadá
Doutorado pela Faculdade de Medicina da USP
Endereço para correspondência: Dr. Ricardo Miranda
Rua Groenlândia, 906, Jardim America 01434-000 – São Paulo, SP
email: drmiranda78@gmail.com
São Paulo, 2026
Prefácio
A 7ª edição do e-book Doenças do Silicone tem o compromisso de sempre se manter atualizado.
Ao longo dos 7 anos de atualização do e-book, é possível perceber a quantidade expressiva de publicação em revistas de renome sobre o tema de doenças do silicone e explante de prótese de mama.
O paciente que procura o cirurgião para o explante não quer ser julgado, mas ouvido, compreendido e acolhido. Boa leitura!
Sumário
SÍNDROME ASIA 7
INTRODUÇÃO 7
SINTOMAS 8
DIAGNÓSTICO 8
PACIENTES DE RISCO 9
MECANISMO DA DOENÇA 10
CONTROVÉRSIAS 10
TRATAMENTO 11
PRÉ-OPERATÓRIO 15
PÓS-OPERATÓRIO 17
RISCOS ASSOCIADOS À CIRURGIA 17
DOENÇA DO SILICONE
BREAST IMPLANT ILLNESS (BII) 19
INTRODUÇÃO 19
MECANISMO DA DOENÇA DO SILICONE 20
CONTROVÉRSIAS 21
DIAGNÓSTICO 23
SINTOMAS 24
RECOMENDAÇÕES DA U.S. FOOD AND DRUG ADMINISTRATION 26
PACIENTE DE RISCO PARA DOENÇA DO SILICONE 27
TRATAMENTO 28
POR QUE RETIRAR AS CÁPSULAS DAS PRÓTESES DE MAMA? 29
LINFOMA ANAPLÁSICO DE CÉLULAS GRANDES 30
INTRODUÇÃO 30
SINTOMAS 31
DIAGNÓSTICO 31
MECANISMO DA DOENÇA 33
PRÉ-OPERATÓRIO 34
TRATAMENTO 34
PÓS-OPERATÓRIO 36
COMPLICAÇÕES MECÂNICAS EM PRÓTESES MAMÁRIAS 37
CONTRATURA CAPSULAR 37
RUPTURA DAS PRÓTESES 41
SEROMAS 43
DUPLA CÁPSULA 45
DEFORMIDADE EM PROTESE SUBMUSCULAR 46
GRANULOMA INDUZIDO POR SILICONE (SIG-BIC) 51
RECONSTRUÇÃO DE MAMA APÓS O EXPLANTE 53
REFERÊNCIAS 56
SÍNDROME ASIA
Introdução
Síndrome ASIA é a abreviação em inglês de síndrome autoimune induzida por adjuvantes. Adjuvantes são todos os materiais estranhos ao organismo que podem desencadear um processo inflamatório crônico, ou seja, um processo que continua por um longo período.
Descrita em 2011 pelo médico israelense Yehuda Shoenfeld, a síndrome engloba doenças autoimunes que apresentam sintomas parecidos desencadeadas por adjuvantes.(4) As doenças descritas e seus agentes desencadeadores são: siliconoses (silicone), síndrome da miofasciíte macrofágica (hidróxido de alumínio), síndrome da Guerra do Golfo (esqualeno) e fenômenos pós-vacinação (hidróxido de alumínio). Outras substâncias também podem ser associadas a essa síndrome, como iodo, mercúrio, óleo mineral, titânio e outros.(5, 6)
O silicone foi introduzido na medicina em 1947 por meio do uso de curativos e desde então tem sido usado em diversos materiais e próteses. Inicialmente foi considerado uma substância inerte, estável, com consistência que imitava o tecido humano e resistente a degradação.(7, 8)
Após o início do uso do silicone na medicina, alguns estudos apontaram que quando injetado desencadeava reações locais graves e que o silicone aparecia em locais distantes da região aplicada, sugerindo que o material não era imunologicamente inerte como se acreditava.(9, 10)
Evidências mostram a associação da inclusão de prótese de mama e doenças relacionadas com o implante desde a década de 1960, logo após o uso das próteses mamárias de silicone em reconstruções e cirurgias estéticas.(11) Alguns estudos, ainda que de forma inconclusiva, demonstraram que pacientes com prótese de mama têm risco aumentado de artrite reumatoide, síndrome de Sjogren, síndrome de Raynaud e esclerodermia.(12)
Sintomas
Os sintomas mais comuns são artrites, mialgias, fadiga e manifestações neurológicas. No Quadro 1 estão representados os possíveis sintomas relacionados à síndrome ASIA(13). Normalmente esses sintomas aparecem após alguns anos da inclusão da prótese de mama.
Quadro 1. Sintomas da síndrome ASIA
Mialgia, miosite, fraqueza muscular
Distúrbios do sono Alteração do humor
Fadiga crônica Sensibiidade à luz e som Sintomas de fibromialgia
Alterações cognitivas, perda de memória Perda de cabelo Falta de ar
Febre Pele e cabelo secos Transpiração noturna
Boca e olhos secos Dor de cabeça Infecção genital
Ansiedade Depressão Lesões na pele
Fonte: autoria própria
Diagnóstico
Para se chegar ao diagnóstico, é necessário que haja ao menos dois critérios maiores ou um critério maior e dois menores dos sintomas (Quadro 2).(4) Por exemplo, uma paciente que tenha artrite após inclusão de prótese de mama se enquadra no diagnóstico de síndrome ASIA. O diagnóstico é essencialmente clínico, por meio de exame físico e história médica. Não há marcadores laboratoriais específicos para o diagnóstico da síndrome ASIA.
Quadro 2. Critérios diagnósticos da Síndrome ASIA
Critérios maiores
Presença de manifestação clínica
-Artralgia ou artrite
-Manifestações neurológicas
-Febre, boca seca
Biópsia de órgãos envolvidos com alterações típicas
Critérios menores
Outras manifestações como síndrome do intestino irritável
Aparecimento de doenças autoimunes (ex.: esclerodermia) Fonte: Shoenfeld, 2011
Pacientes de risco
Pode ocorrer em pacientes que tenham próteses de mama íntegras ou rompidas. O silicone da prótese mamária pode ser achado em regiões distantes da mama, como os linfonodos. Têm se observado que, quanto maior o tempo que o paciente está com a prótese, maior o risco de desenvolver a doença.
Os pacientes com maiores riscos de desenvolver síndrome ASIA são aqueles com:(1)
• Deficiência da vitamina D(2)
• Relato de reação autoimune a adjuvantes (silicone, vacinação)
• Condições autoimunes diagnosticadas (ex.: artrite reumatoide, esclerodermia)
• História de alergia e doenças atópicas
• Predisposição a desenvolver doença autoimune (história familiar de doenças autoimunes)(3)
Mecanismo da doença
A doença ocorre devido à presença de materiais estranhos no corpo, os adjuvantes, que desencadeiam uma inflamação crônica e a liberação de substâncias inflamatórias.(3)
Essas substâncias inflamatórias desencadeadas pela presença de corpo estranho ocasionarão os sintomas relacionados da doença, como artralgia, fadiga e febre, dentre outros.
Controvérsias
A maior crítica em relação à síndrome ASIA está relacionado aos critérios diagnósticos, pouco específicos e muito abrangentes. Dessa forma, os
critérios diagnósticos podem incluir pacientes com outras doenças reumáticas ou autoimunes.(14)
Outra controvérsia se refere ao próprio mecanismo da doença. Há um artigo que defende que o mecanismo da doença ocorra pela toxicidade do próprio silicone no organismo e não pela resposta autoimune desencadeada pelo corpo estranho.(15) Há também o argumento da exposição ao longo da vida a outros tipos de adjuvantes, além do silicone, que poderiam desencadear a doença.(16)
Por fim, alguns autores questionam se a prótese de mama pode ser adjuvante mesmo estando íntegra ou somente nos casos em que há ruptura. Ao longo dos anos pode haver exposição ao silicone presente em outros produtos além do implante mamário, sendo mais uma dificuldade para se identificar o implante como adjuvante.(17) Apesar do aumento da publicação referente a esse tópico, a Síndrome ASIA se mantém controverso no meio médico e comunidade científica.(18)
Tratamento
O tratamento pode ser somente cirúrgico ou associado à medicação que diminua o processo inflamatório, como corticoides, imunossupressores e medicações biológicas (ex.: adalimumabe). Raramente o tratamento será somente medicamentoso.
O tratamento cirúrgico preconizado para paciente que apresente os sintomas é a retirada da prótese em conjunto com a sua cápsula, comumente chamado “explante em bloco”. Ao longo dos anos, o organismo cria uma cápsula em torno da prótese, sendo este um processo normal. A cápsula é uma estrutura de colágeno formada em torno da prótese mamária, ocorrendo normalmente em todas os pacientes com prótese. O termo mais correto seria capsulectomia total intacta, mas explante em bloco ficou popularizado pela mídia social.(19)
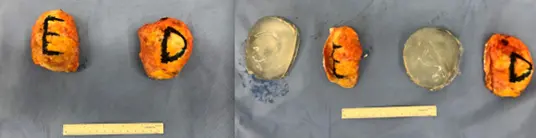
Nos casos de síndrome ASIA, é necessário retirar toda a cápsula, pois ela pode apresentar resquícios da prótese de silicone e se evita a contaminação dos tecidos mamários por silicone nos casos de ruptura. Nos laudos de anatomia patológica da cápsula, é possível verificar alterações normais frente à prótese de mama (Figura 1) e evidência de silicone nas cápsulas (Figura 2).(20)
Figura 1. Resultados considerados normais para biópsia de cápsula de prótese de mama. Fonte: elaborada pelo autor.

Figura 2. Evidência de material de prótese mamária (silicone) na biópsia da cápsula. Fonte: elaborada pelo autor.
Há muita confusão em relação aos termos utilizados na cirurgia de retirada de implante e cápsula. As definições mais comumente utilizadas são:
• Capsulotomia: a cápsula é incisada para que haja aumento do tamanho da loja, do espaço em que estava a prótese prévia. Neste caso a cápsula não é retirada.
• Capsulectomia parcial: retirada de parte da cápsula.
• Capsulectomia total: retirada total da cápsula. Muitos cirurgiões utilizam capsulectomia total e explante em bloco como sinônimos, mas na capsulectomia total não está necessariamente implícito que a cápsula e a prótese serão retiradas em bloco. Na capsulectomia total o cirurgião pode abrir a cápsula e retirar a prótese para posteriormente realizar a retirada de toda a cápsula.
• Capsulectomia total intacta: retirada da prótese e da cápsula em uma única peça, sem rompimento da cápsula e sem contaminação do silicone no campo cirúrgico. É a cirurgia preconizada no tratamento de doenças associadas ao implante de silicone (Figura 2).
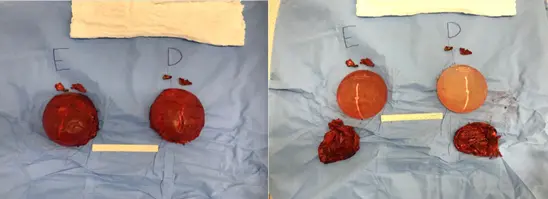
• Explante em bloco: termo mais corretamente empregado nos casos de linfoma anaplásico de células grandes, em que a prótese e a cápsula são retiradas em uma peça única, mas com uma margem de segurança, ou seja, retirando-se um pouco de tecido ao redor da cápsula para garantir que nenhuma célula de tumor fique na mama (Figura 3).
Pré-operatório
Pré-operatório: principais dúvidas
Pós-operatório
Riscos associados à cirurgia
DOENÇA DO SILICONE – BREAST IMPLANT ILLNESS (BII)
Introdução
Outra entidade que não deve ser confundida com síndrome ASIA é o Breast Implant Illness (BII) – ou livremente traduzida como doença do silicone.(24) BII é uma constelação de sintomas reportados pelas pacientes (fadiga, queda de cabelo, ansiedade, depressão, fotossensibilidade, insônia), sem alterações laboratoriais ou radiológicas.(25-27)
A doença do silicone inclui diversos termos, como síndrome autoimune induzida por adjuvantes, síndrome autoimune/inflamatório induzido por adjuvante e síndrome da incompatibilidade do silicone.(28)
Não é uma doença reconhecida pela classe médica. Está associada a todas as marcas e modelos de prótese de mama e pode ocorrer entre 3 dias a 30 anos após a inclusão.(29) O receio de ter sintomas ou complicações devido à prótese de silicone tem levado ao aumento pela procura por explante. Desde 2017 a procura pelo explante subiu 34,4%, enquanto a busca pelo implante de prótese de mama caiu 14,9% nos Estados Unidos.(30) Em 2019, em torno de 33.000 explantes foram realizados nos Estados Unidos.(31)
A associação da prótese de mama com doenças e sintomas não é nova, sendo os primeiros estudos publicados em 1980. Por conta desse receio, em 1992 a U.S. FDA removeu do mercado as próteses de silicone. Muitos estudos tentaram estabelecer uma associação entre prótese de mama e doenças autoimunes ou reumáticas, porém todos inconclusivos.(32) Em um estudo de revisão de literatura, mostrou-se um pequeno aumento de risco de se ter síndrome de Sjogren e artrite reumatoide em pacientes com prótese de mama, mas o próprio estudo reconhece que são necessárias mais evidências para se confirmar essa associação.(33)
Sem confirmar a associação entre a prótese de mama e doenças sistêmicas, as próteses de silicone voltaram ao mercado em 2006 com a condição de que as empresas fabricantes conduzissem estudos de longo prazo para avaliar a segurança do implante.(32)
O movimento para que a doença do silicone seja reconhecida como uma entidade médica ganhou força por meio das organizações de pacientes em mídias sociais altamente engajadas e estruturadas. Mas as mídias sociais podem causar uma escalada de preocupações baseadas em sintomas comuns e inespecíficos, que levam à ansiedade induzida e inquietação compartilhada.(34-36)
Mecanismo da doença do silicone
Há diversas teorias tentando explicar a razão pela qual a prótese de mama pode estar relacionada com diversos sintomas sistêmicos, embora o mecanismo exato ainda seja desconhecido. Investiga-se sobre o mecanismo de inflamação, contaminação bacteriana, toxicidade dos componentes da prótese e exacerbação do sistema autoimune.(32, 37)
Seguem as teorias mais estudadas sobre o mecanismo da doença do silicone.
Síndrome autoimune: reportada incialmente pela literatura japonesa em 1964, ocorre pela resposta exagerada do sistema imune em pessoas com predisposição genética frente a um corpo estranho. A resposta autoimune exagerada leva à inflamação crônica, resultando em aumento dos sintomas alérgicos, imunodeficiência e doenças autoimunes.(38, 39)
Biofilme: são agrupamentos de bactérias firmemente grudadas em superfícies de tecido humano ou implantes médicos compostos de diversos materiais. Os biofilmes causam uma inflamação crônica local que pode ser responsável pela contratura capsular e BIA-ALCL. A bactéria mais comumente associada é o Propionibacterium acnes, conhecida também por Cutibacterium acnes, normalmente presente na pele.(28)
Toxicidade do silicone: pequenas moléculas do silicone podem vazar da prótese e eventualmente aparecer em outros órgãos, mais comumente nos linfonodos axilares. O silicone em outros órgãos pode estimular uma reação inflamatória e até morte celular. Para fazer a prótese de silicone são utilizados metais pesados, que também podem ser tóxicos caso apareçam em outros órgãos.(12, 40, 41)
Psicossomático: os sintomas da doença do silicone podem ser uma entidade psicossomática chamada de desordem somática sistêmica caracterizada pela amplificação de sintomas comuns, sofrimento e desabilitação sem uma causa identificável.(42)
Fenômeno da mídia social: as informações disponíveis nos grupos sociais podem aumentar a ansiedade e o medo de se manter a prótese de silicone, levando pessoas a se autodiagnosticarem com doença do silicone.
Outros mecanismos: os sintomas da doença do silicone se parecem com os da síndrome da fadiga crônica, lesão por esforço repetitivo, fibromialgia e sintomas de sarcoidoses (doença autoimune desencadeada por corpo estranho).(43)
Controvérsias
A doença do silicone é um tema polêmico e muito discutido na comunidade médica. Ainda há muito o que se pesquisar para se provar cientificamente qual a relação entre o implante de silicone e os sintomas sistêmicos relatados pelos pacientes. Muitos pacientes têm confiado mais nas informações de amigos(as) e da mídia social do que nas palavras do médico especialista. Têm-se discutido qual a razão dessa falta de confiança. Alguns pacientes se sentem frustrados por não acharem um motivo para seus sintomas, e menos ainda um tratamento.(44, 45)
Tendo passado por diversas especialidades médicas, os pacientes se tornam desacreditados nos médicos e na medicina convencional. Cabe lembrar que a mídia social serve como uma comunidade para troca de experiências e suporte, algo não encontrado nas consultas médicas.
É nesse sentido que a comunidade médica tem que se esforçar para melhorar a comunicação com o paciente e ser bem clara em relação aos benefícios e riscos associados a qualquer procedimento cirúrgico.(46)
Uma incoerência encontrada é que os sintomas da doença do silicone não aparecem em pacientes com outros implantes de silicone no corpo que não o mamário.(47)
Em um estudo, não foi achado evidência de associação entre prótese de mama e doença do silicone em pacientes que foram submetidas à reconstrução de mama após mastectomia por tumor.(48)
Os pacientes também compartilham características psicológicas e sintomáticas de outras doenças, como fibromialgia, desordem somática sistêmica, ansiedade e síndrome da fadiga crônica. As causas dos sintomas são atribuídas a um corpo estranho, levando à somatização ou fixação psicológica. Avaliação psiquiátrica deve ser solicitada nesses casos, uma vez que somente o explante pode não beneficiar essas pacientes.(30, 42, 49-51)
Foi identificado resíduos metais provenientes dos implantes mamários em tecidos e sangue de pacientes, o principal elemento sendo a platina. No entanto, o nível desses metais é abaixo do limite de toxicidade e não há evidências que mostrem associação com os sintomas relacionados à doença do silicone.(12, 52)
Mesmo em pacientes com próteses rompidas e maior exposição ao silicone, não foi achado maior risco de terem sintomas relacionados à doença do silicone. Aparentemente, a integridade da prótese tem pouco impacto no aparecimento de sintomas clínicos.(12)
Uma grande controvérsia existe se na retirada da prótese deve-se obrigatoriamente remover a cápsula.(31)
Há pouca evidência científica justificando a capsulectomia total ou em bloco em pacientes com doença do silicone. Há benefícios da capsulectomia em pacientes com contratura avançada, como a diminuição do risco de seromas, das cápsulas serem palpáveis ou identificáveis em exames de imagem e pela diminuição do risco de retenção de silicone nas cápsulas.(53-56)
As contraindicações relativas de capsulectomia envolvem cápsulas finas, cápsulas muito aderidas às costelas quando a prótese é submuscular e casos de simastia (Figura 5).(29, 57-61)
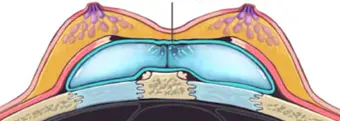
Figura 5. Caso de simastia pelo encontro das próteses na frente do esterno, dando a impressão de que as mamas não são separadas. Fonte: Guillier et al., 2020.
Em um artigo de revisão, foi concluído que a maior indicação da capsulectomia total é devido à contratura capsular avançada. O autor não encontrou evidências científicas para capsulectomia total como um modo de diminuir chances de ter BIA-ALCL ou diminuição dos sintomas de doença do silicone. O explante em bloco está formalmente indicado em casos confirmados ou suspeitos de BIA-ALCL.(57)
Diagnóstico
Muitos pacientes se autodiagnosticam com doença do silicone e não levam em consideração que os sintomas podem ser multifatoriais ou ainda relacionados a outras doenças reumáticas (ex. fibromialgia) ou autoimunes (ex. tireoidite de Hashimoto).(62, 63) Deve-se pensar também em transtornos somatoformes ou transtornos de desordem somáticos, que consistem em preocupação excessiva e desproporcional frente a sintomas, acarretando ansiedade em pacientes mesmo que evidências médicas demonstrem que não estão doentes.(64-66) Doença do silicone e Síndrome ASIA são entidades diferentes, embora apresentem muitos sintomas parecidos (Quadro 3).
Quadro 3. Diferenças entre síndrome ASIA e doença do silicone
Diagnóstico
Exame específico
Doença reconhecida
Mecanismo de ação
Exclusivo do silicone
Doença do silicone
Sintomas Não Não Desconhecido Sim diversos
Sintomas
Os sintomas mais comuns reportados pelos pacientes de grupos de doença do silicone são fadiga, dores musculares e articulares, problemas cognitivos (como falta de memória), problemas no sono, queda de cabelo, infecções recorrentes, manchas cutâneas, problemas de tireoide e adrenais. Os sintomas normalmente se desenvolvem após 6 anos da inclusão de prótese de mama e o explante ocorre em média após 12 anos da implantação.(39)
Há estudo que relaciona o implante de prótese de mama com o desenvolvimento de Transtorno de Sintomas Somáticos (TSS). O diagnóstico do TSS é baseado na presença de ansiedade e presença persistente de pensamentos e preocupações com sintomas. A duração das queixas dura ao menos 6 meses e são excessivas e desproporcionais em relação à gravidade dos sintomas.(67)
A doença do silicone deve ser um diagnóstico de exclusão, e todo esforço aplicado na busca de outras doenças que compartilham os mesmos sintomas. Por isso é importante encaminhar o paciente para outros especialistas além do cirurgião plástico. O cuidado ao paciente com diversos sintomas exige uma equipe multiprofissional (Quadro 4).(68)
Quadro 4. Profissionais encaminhados de acordo com os sintomas
Sintomas Especialista
Fadiga Cardiologista, hematologista
Problemas cognitivos Neurologista, psiquiatra
Ansiedade Psiquiatra
Dores musculares, articulares Reumatologista, ortopedista Queda de cabelo Dermatologista
Alguns sites de apoio ao implante relacionam a presença de genes HLA B27, HLA DR52 e HLA DR53 ao fato de o paciente ter maior sensibilidade ao silicone e probabilidade de desenvolver sintomas.(69, 70)
Há diversos estudos relatando melhora a longo prazo dos sintomas da doença do silicone após o explante.(12, 53) Um estudo demonstrou que houve resolução parcial dos sintomas em 74% dos casos e melhora total dos sintomas em 23% dos casos.(32) Outros mostraram melhora dos sintomas entre 50% e 75% das pacientes. Porém, é sempre importante frisar que há uma parcela das pacientes que relata não ter melhora dos sintomas após o explante.(13, 21, 71, 72)
A presença ou não de doenças psiquiátricas não têm influenciam na melhora dos sintomas após o explante. Pacientes com contratura capsular grave (graus III ou IV) apresentam melhora mais importante nos sintomas mecânicos relacionados à contratura (ex. dores nas mamas) com menor impacto de melhora em outros sintomas sistêmicos (ex. fadiga, dor muscular). Neste estudo, o item mais importante para se evitar sintomas sistêmicos residuais é o tempo entre a inclusão do implante e sua remoção. Desse modo, quanto menor o tempo de implante maiores as chances de melhora dos sintomas sem apresentar queixas residuais relacionadas à prótese.(73)
Ansiedade e depressão são os fatores preditivos mais associados ao desenvolvimento de sintomas da Doença do Silicone em pacientes submetidas à inclusão de prótese de mama. A mídia social amplifica as preocupações dessas pacientes, tendo influenciado a decisão pelo explante em 87% dos casos dessa população.(39)
Um sintoma em particular que tem melhorado consistentemente, mesmo no pós-operatório imediato, é a qualidade da respiração. Pacientes relatam que estão respirando melhor após o explante. Embora muitos tenham esse benefício subjetivo, não foi possível provar que a retirada da prótese aumenta a função pulmonar.(74) Uma das explicações para esse benefício seria que a retirada do peso alivia o peso na caixa torácica, do mesmo modo que ocorre em uma cirurgia de redução de mamas.(75)
Recomendações da U.S. Food and Drug Administration (U.S. FDA)
A U.S. Food and Drug Administration, nos Estados Unidos, é o órgão equivalente à Agência Nacional de Vigilância Sanitária (Anvisa) no Brasil, ou seja, é uma agência reguladora ligada ao governo federal que atua no controle de diversos produtos, como alimentos, medicamentos e os que envolvam risco à saúde.
Em setembro de 2020, após anos de ativismo de pessoas envolvidas nestes problemas, a U.S. FDA indicou uma orientação aos fabricantes de colocarem avisos nas embalagens de prótese de mama sobre os efeitos negativos do implante,(76) a saber:
• As próteses de mama não são vitalícias. As chances de haver necessidade de troca devido a complicações aumentam com o tempo.
• As próteses de mama têm sido associadas a um tipo de tumor do sistema imune chamado linfoma anaplásico de células gigantes. Esse tipo de tumor está mais relacionado a próteses texturizadas do que lisas.
• Pacientes com prótese de mama podem se queixar de sintomas sistêmicos como dores musculares, dores articulares, fadiga e outros sintomas. O risco individual de cada paciente desenvolver esses sintomas não está bem estabelecido. Alguns pacientes relatam resolução completa dos sintomas após retirada de prótese sem a inclusão de novo implante.
Além disso, há a questão do gel bleed, que é o extravasamento de pequenas partículas de silicone pelo invólucro da prótese e o acúmulo em diversos órgãos. Isto porque, como já mencionado, a prótese de mama possui diversos metais pesados e substâncias tóxicas utilizadas na fabricação da mesma.(70)
Em setembro de 2022, a U.S. FDA publicou que, após revisão da literatura médica, foram identificados menos de 20 casos de carcinoma espinocelular e menos de 30 de linfomas nas cápsulas dos implantes. A U.S. FDA orienta que pacientes com próteses de mamas sejam informadas sobre estes riscos, embora raros.
A U. S. FDA recomenda ainda que o acompanhamento de pacientes com prótese de mama seja realizado com ressonância nuclear magnética e comece 5 a 6 anos após a cirurgia, com periodicidade de 2 a 3 anos após o primeiro exame. Em pacientes assintomáticos, a ultrassonografia de mamas é uma alternativa aceitável.(76)
Por outro lado, estudos mostram que há melhora dos sintomas ao se realizar o explante. Essa melhora pode se dar pela retirada do objeto de somatização e ansiedade, efeito placebo ou de fato pelos mecanismos de inflamação crônica e autoimune.(53) Em alguns casos essa melhora é incompleta e passageira, sendo necessário acompanhamento com equipe multiprofissional.(77)
Paciente de risco para Doença do Silicone
Há alguns indivíduos que possuem predisposição para uma resposta autoimune quando expostos à materiais e corpos estranhos. Esses indivíduos de maior risco foram relacionados à presença genética de certos tipos de HLA (do inglês antígeno leucocitário humano) como o HLA-DR5, HLA-DQ2, HLA DRB1 e HLA DQB1. O HLA é a identidade do sistema imune de uma pessoa.(39)
O aumento de produção de autoanticorpos, especialmente o anticorpo antinuclear (ANA), se normaliza após o explante de prótese de silicone, sugerindo uma relação do aumento desses anticorpos nas pacientes com prótese em relação à população controle.(39)
As doenças autoimunes, dentre elas fibromialgia, é considerada um fator de risco para desenvolvimento de doença do silicone. A presença de biofilme, um tipo de capa de bactéria envolvendo a prótese, também está relacionado à inflamação crônica da cápsula e desenvolvimento de sintomas sistêmicos. Por fim, as redes sociais.
Tratamento
O tratamento do BII deve ser bastante individualizado e no momento o diagnóstico tem que ser de exclusão. Énecessário fazer umaintensa investigação multidisciplinar para tentar definir ou excluir outras doenças que possam causar os mesmos sintomas. Feita essa investigação, é necessário que o cirurgião plástico informe ao paciente que oexplante em bloco pode não melhorar o quadro.(78)
Após a cirurgia, pode haver alguns cenários: melhora significativa de todos os sintomas no longo prazo, melhora significativa departe dos sintomas no longo prazo, melhora dos sintomas por um período e depois recidiva ou sem melhora dos sintomas em nenhum período. A melhora dos sintomas pode ocorrer em até 6 a 12 meses da cirurgia e, após esse período, a chance de ocorrer alguma melhora é pequena.(79)
De acordo com um artigo de revisão de literatura, 81,9% dos pacientes que relatavam sintomas de doença do silicone tiveram melhora das queixas. A redução foi de 55,1% dos sintomas, ou seja, houve melhora em mais da metade dos sintomas relatados. Estudos revelam que a retirada da prótese, com ou sem capsulectomia total, leva aumamelhora ou resolução dos sintomas.(39)
Por que retirar as cápsulas das próteses de mama?
Nas cápsulas mamárias há um tipo especial de célula chamada miofibroblasto, responsável pela contratura capsular. Nas cápsulas são encontrados fragmentos de silicone no espaço extracelular ou dentro de células especializadas como os histiócitos e células gigantocelulares.(80)
A cápsula pode ser fina, espessa, nodular, calcificada ou dupla. A metaplasia sinovial encontrada nas biópsias é uma adaptação do organismo devido ao movimento da prótese em torno do tecido mamário. A retirada das cápsulas nos casos de contratura mais grave é necessária para evitar seromas e palpabilidade.(81, 82)
A cápsula deve ser enviada à anatomia patológica para análise, considerando que a incidência de BIA-ALCL é de 0,03% a 0,05% em pacientes com próteses texturizadas. Outros tumores também podem ser diagnosticados, como o carcinoma invasivo (0,16%), carcinoma ductal in situ (0,16%) e carcinoma lobular in situ (0,04%).(83)
Não há diferença histológica (inflamação, fibrose, reação de corpo estranho) entre as cápsulas das próteses de mama de pacientes com sintomas de Doença do Silicone e pacientes sem sintomas. Esse achado não suporta a hipótese de que os sintomas são causados pelas alterações histológicas das cápsulas e portanto coloca em dúvida a necessidade de capsulectomia total em todas as pacientes.(84)
A presença de partículas de silicone nas cápsulas é principalmente devido ao conteúdo das próteses e não pelo invólucro dos implantes. Essa conclusão é devida à maior presença de resíduos de silicone em implantes de silicone quando comparado aos implantes salinos.(85)
A bactéria comensal mais comumente achada nos biofilmes é o
propionibacterium.(86-88)
LINFOMA ANAPLÁSICO DE CÉLULAS GRANDES
Introdução
O linfoma anaplásico de células grandes associado ao implante de prótese de silicone (BIA-ALCL) é um tumor que foi descrito há mais de duas décadas, mas que somente a partir de 2016 começou a receber a atenção dos médicos e da mídia.(89, 90)
É um linfoma não-Hodgkin de células T, responsáveis pela resposta imune. A incidência é estimada em um para 30.000 pacientes com implantes texturizados. Até junho de 2023 foram reportados à U.S. FDA
1.264 casos de BIA-ALCL com 63 mortes ao redor do mundo.(91-93) A prevalência do BIA-ALCL é estimada em 0,03% para pacientes com implantes texturizados e de 0,0067% para paciente com próteses de qualquer modelo.(94)
Um outro tumor associado ao implante mamário é o carcinoma de células escamosas nas cápsulas dos implantes, embora seja um tumor extremamente raro com somente 19 casos descritos na literatura médica e três mortes relatadas.(93)
O primeiro caso relatado do BIA-ALCL foi descrito por Keech e Creech, em 1997, mas somente em 2011 a U.S. FDA lançou um aviso sobre a relação entre a prótese de silicone e a doença. Em julho de 2019, o órgão solicitou que a fabricante de próteses de mama Allergan voluntariamente removesse os implantes texturizados, devido a um risco maior de BIA- ALCL.(95)
É considerado um tumor raro e se apresenta normalmente como uma coleção de líquidos em volta da prótese ou da cápsula. Segundo um estudo, a incidência é de um caso em cada 500.000 pacientes com prótese de mama. A idade acometida varia entre 34 a 59 anos, com média de 46 anos; a doença pode se desenvolver entre 3 e 7 anos após a inclusão de prótese mamária.(96)
O BIA-ALCL ocorre em próteses texturizadas, ou seja, que têm a superfície rugosa. Não foi encontrada associação com próteses lisas.(97, 98)
Sintomas
A apresentação clínica mais comum foi a presença rápida e espontânea de líquido (seroma) tardio em volta da prótese associado ao aumento do volume mamário, dor e contratura capsular. Esses sintomas ocorreram em média de 8 a 10 anos após a cirurgia.(99, 100)
Sintomas menos frequentes incluem vermelhidões na pele, endurecimento das mamas por contratura capsular e presença de nódulos no corpo por aumento dos linfonodos.(101)
A presença de líquido nas mamas, também conhecida como seroma, é um sintoma tão importante que qualquer seroma que ocorra após 1 ano da inclusão de prótese de mama deve ser suspeito para linfoma anaplásico de células grandes. Nos seromas que ocorrem menos de um ano após a cirurgia de implante, outras causas devem ser levantadas como trauma ou infecção.(102)
A apresentação dos sintomas tem uma característica bimodal, sendo que pode se dar por meio de seromas tardios e relacionados a casos menos graves. Outra apresentação é pela identificação de um tumor em torno da prótese e está relacionada a doenças mais graves.(91)
Diagnóstico
O tempo médio da inclusão do implante para o diagnóstico de BIA-ALCL foi de 8 anos, embora haja relatos de diagnóstico da doença entre 1 e 34 anos da cirurgia.(100)
Os exames mais comumente solicitados visam a identificar líquido em torno da prótese e tumorações na mama. Para identificar a presença de líquido, a ultrassonografia é um exame adequado. A ressonância nuclear magnética é utilizada para se avaliar melhor a prótese e eventuais tumores nas mamas.(103)
O líquido em torno da prótese deve ser aspirado através de uma punção auxiliada por ultrassonografia. Esse procedimento pode ser realizado em clínica ou laboratório. No caso de tumoração na mama, linfonodo palpável ou cápsula com contratura grau IV, o material retirado deve ser enviado para anatomia patológica, citologia (pesquisa de células anaplásicas gigantes), imuno-histoquímica (CD30 e ALK) e cultura para verificação de bactérias.(104)
Caso o diagnóstico se confirme na presença de células atípicas (anaplásicas) e imuno-histoquímica positiva para CD30 e negativa para ALK, também deverá ser realizado o exame de PET-Scan (PET-CT – tomografia por emissão de pósitrons) para investigação de tumores em outras partes do corpo.(91, 104)
O líquido aspirado tem um aspecto amarelado e sanguinolento, como observado na Figura 6. Há protocolos definidos para conduzir a investigação de BIA-ALCL (Figura 7).(97, 105)

Figura 6. Retirada de líquido da mama auxiliado por ultrassonografia (foto esquerda). Aspecto do líquido retirado. Fonte: Gidengil CA et al., 2015.
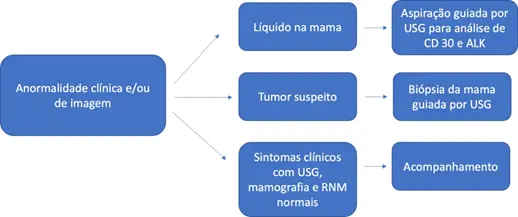
Figura 7. Protocolo para pesquisa de linfoma anaplásico de células grandes (BIA- ALCL). Fonte: Colwell A.S., 2021.
USG: ultrassonografia; RNM: ressonância nuclear magnética
Mecanismo da doença
Há diversas teorias e estudos sendo conduzidos para melhor esclarecimento da relação entre a prótese de mama texturizada e o linfoma.(106)
A teoria mais aceita é de que a prótese de mama estimula um processo inflamatório crônico que leva à proliferação de células específicas, células T, e ao desenvolvimento do tumor em pacientes geneticamente susceptíveis.(107)
Embora haja artigos recomendando a retirada de implante de mama com macrotextura devido ao aumento de desenvolvimento de BIA-ALCL, muitos autores recomendam o acompanhamento anual com exames de imagem antes de realizar um explante profilático.(108)
Pré-operatório
Depois da confirmação, é recomendado passar em consulta com oncologista e, em alguns casos, com cirurgião oncológico. Pode ser que outros exames de imagem ou laboratoriais sejam solicitados para definir melhor o tumor ou excluir tumores em outros locais. Na maioria dos casos o tumor é limitado à cápsula.
Tratamento
Na maior parte dos casos, o procedimento cirúrgico é o suficiente para o tratamento do linfoma, que consiste na retirada da prótese e de toda a cápsula e de eventuais tumores aderidos à cápsula. A apresentação é bimodal, ou seja, na maioria dos casos o tumor estará restrito à cápsula da prótese, porém há casos de tumores em outros órgãos.(91)
O ideal é realizar o explante em bloco, ou seja, retirar a prótese e toda a cápsula em uma só peça. Em alguns casos, principalmente naqueles que a prótese está atrás do músculo, é retirada toda a cápsula (capsulectomia total), porém não em bloco. Pode ser necessário retirar linfonodos e tumores aderidos à cápsula.(109)
Nos casos iniciais do linfoma (estádios I e II), a reconstrução da mama pode ser feita imediatamente após o explante em bloco, porém nos casos mais avançados (estádios III e IV) deve ser postergada por 5 anos.(104)
Deve ser considerada a retirada do implante e da cápsula na mama sem doença, já que há risco aumentado de linfoma na outra mama também.(109)
A gravidade do tumor pode ser classificada em estádios, que vão de I até IV. São considerados tumores menos graves os com estádios I e II e mais avançados os de estádio III e IV.
Os casos primários e menos graves de BIA-ALCL (estádios I e II) têm boa resposta ao tratamento cirúrgico, com altas taxa de sobrevida sem a doença. A taxa de cura é acima de 90% em casos diagnosticados precocemente e com realização de explante em bloco de prótese e cápsula mamária.(110, 111)
Nos casos com a doença avançada (estádios III e IV), que apresentem metástase nos linfonodos, será necessário, além da cirurgia, o uso de quimioterapia e radioterapia.(112)
No estádio I o tratamento padrão é a retirada da prótese com capsulectomia em bloco. Se na anatomia patológica constatar que todo o tumor foi retirado com margens livres, o paciente estará curado (Figura 8).
No estádio II, o tratamento também inclui a retirada da prótese com capsulectomia em bloco, mais retirada do tumor adjacente à cápsula e linfadenectomia (retirada de linfonodos). Nos casos de comprometimento do linfonodo é necessário realizar quimioterapia e/ou imunoterapia no pós-operatório.
Nos estádios mais avançados (estádios III e IV) é necessário um acompanhamento multidisciplinar (oncologista, cirurgião torácico, cirurgião plástico, cirurgião oncológico) para o planejamento do tratamento. É realizada a retirada do implante com capsulectomia em bloco, retirada de tumores a distância, linfadenectomia, biópsia de medula óssea e quimioterapia, imunoterapia e/ou radioterapia.(104)
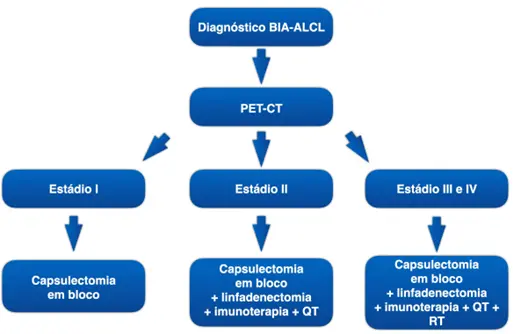
Figura 8. Tratamento do BIA-ALCL conforme estádio. Fonte: Longo B. et al, 2022.
PET-CT: tomografia por emissão de pósitrons; QT: quimioterapia; RT: radioterapia
Em todos os estádios o acompanhamento será feito com exames de imagem a cada 3 a 6 meses nos primeiros 2 anos e depois anualmente até se completar 5 anos.
Pós-operatório
O pós-operatório envolve repouso por 2 a 4 semanas, uso de sutiã cirúrgico por 2 meses e acompanhamento com o cirurgião plástico.
Será necessário realizar um acompanhamento em conjunto com oncologista, no qual será feito um monitoramento para verificar se há recidiva do tumor. Pacientes terão que ser acompanhados a cada 6 meses por 2 anos e depois anualmente por pelo menos 5 anos.
COMPLICAÇÕES MECÂNICAS EM PRÓTESES MAMÁRIAS
As complicações mecânicas são o principal motivo para o desejo da troca ou retirada das próteses e cápsulas. Elas podem ocorrer em qualquer período após a inclusão de prótese de mama, embora os riscos aumentem após 10 a 15 anos da cirurgia. A prótese demama não évitalícia, tendo vida útil em torno de 15 anos.(113,114)
Em um período de 15 anos, 50% dos pacientes com prótese de mama terão que passar por uma cirurgia de revisão devido a dor, questões estéticas ou complicações mecânicas, como contratura capsular ou ruptura.(115)
Contratura capsular
A formação de uma cápsula em torno da prótese é uma reação esperada do organismo frente a um corpo estranho desencadeando um processo inflamatório crônico. Esse processo inflamatório leva à migração de células que depositam colágeno e outras substâncias, criando a cápsula e isolando a prótese do organismo.(99,116)
Algumas dessas células responsáveis pela criação da cápsula adquirem características de células musculares, possuindo a capacidade de se contrair. Ao longo dos anos, essas células modificadas são responsáveis pela contração da cápsula, levando às contraturas capsulares.(117)
As taxas de contratura capsular variam entre 2,8 e 18,9% após 5 a 10 anos da inclusão de prótese de mama. A recorrência da contratura capsular em pacientes que se submetem a uma nova inclusão de prótese de mama é em torno de 18,1 a 39,7%. A troca de plano para loja submuscular e o uso de matriz dérmica acelular podem reduzir a incidência de contratura capsular.(118)
Há uma maior associação da contratura em pacientes com próteses lisas quando comparadas às próteses texturizadas.(39)
A formação da cápsula é uma resposta inflamatória a um corpo estranho. Ela é útil em condições normais para manter a prótese bem- posicionada, mas pode ser dolorosa nos casos de formação fibrótica exagerada, levando à contratura capsular acentuada.(119, 120)
Os potenciais riscos para uma contratura grave são radioterapia, tempo das próteses, implantes texturizados, hematomas no pós- operatório e infecções. Próteses lisas ou com nanotextura estão associadas a menores incidências de contratura capsular.(121, 122)
A contratura pode ser classificada segundo sua gravidade. A classificação de Baker é a mais utilizada e estadia a contratura em graus de I a IV (Quadro 5).(123)
Quadro 5. Classificação de Baker de contratura capsular
Grau Contratura Aparência da mama
II Leve Endurecida quando comparada à mama normal;
prótese palpável, mas não visível
IV Grave Muito endurecida e dolorosa, importante distorção
da anatomia da mama
Fonte: Rotatori DS et al., 1991
Os graus I e II são os mais leves (Figura 9) e não precisam de tratamento. Os graus mais avançados, III e IV (Figura 10), necessitam de tratamento cirúrgico, envolvendo a retirada da prótese em bloco ou a capsulectomia total. A necessidade ou não da mastopexia dependerá da flacidez mamária.(124)
A bactéria presente no biofilme da prótese tem um impacto importante na formação da contratura capsular, sendo que as bactérias mais comuns são Staphylococcus Epidermidis, Cutibacterium Acnes e Estafilococos Coagulase negativo. A teoria é de que a bactéria presente nos biofilmes cause uma resposta inflamatória exacerbada que ocasiona a contratura capsular. A contaminação da prótese pelas bactérias ocorre no momento de inserção na mama. Os biofilmes são bactérias alojadas em uma matriz extracelular de polímero em uma superfície.(125-128)
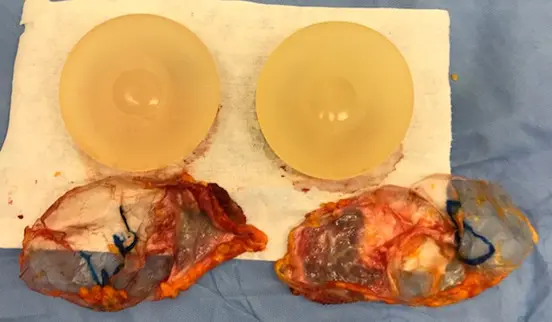
Figura 9. Contratura grau I, cápsulas finas. Fonte: acervo do autor.

Figura 10. Contratura Grau IV, cápsulas espessas, prótese com revestimento de poliuretano. Fonte: Acervo do autor.
Além do tratamento cirúrgico para os casos mais graves de contratura (graus III e IV), algumas medidas não cirúrgicas podem ser tomadas para diminuir a incidência de contratura. As medidas de prevenção de contratura no pré e no intra-operatório incluem administrar antibiótico antes da cirurgia, lavar a prótese de mama com antibiótico, lavar as luvas cirúrgicas e utilizar materiais para introdução da prótese que evite contato com a pele (ex.: Keller Funnel®; Figura 11). Nos casos de contratura mais leve, é possível tentar um tratamento farmacológico com anti-inflamatórios, corticoides e outras medicações como o montelucaste.(115)
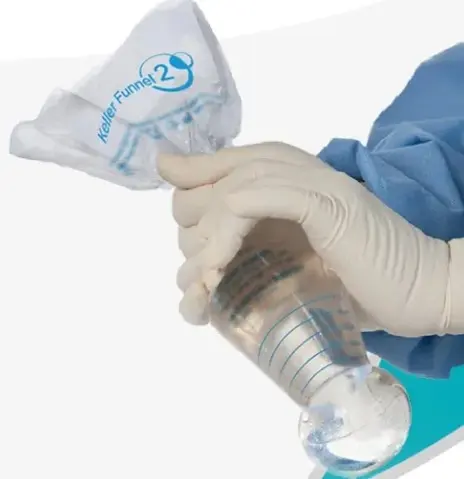
Figura 11. Dispositivo para introdução de prótese de mama. Fonte: www.kellerfunnel.com
Ruptura das próteses
A chance de a prótese se romper aumenta ao longo dos anos e está relacionada à degradação de seu invólucro (Figura 12) e, em alguns casos, a traumas nas mamas. A ruptura pode causar sintomas no paciente como dor e alteração da consistência da mama, mas em alguns casos é assintomática.
A ruptura de prótese de mama pode afetar de 10 a 15% das pacientes que têm o implante entre 10 e 15 anos. Pacientes com implante salina percebem uma diminuição abrupta do volume enquanto pacientes com implante de gel o diagnóstico ocorre com exames de imagem de rotina.(129)
Nas pacientes com queixas sistêmicas compatível com doença do silicone, a ruptura de prótese foi encontrada em 28,5% das pacientes, sugerindo que a integridade da prótese pode influenciar no aparecimento dos sintomas.(39)
O melhor exame para fazer o diagnóstico é a ressonância magnética das mamas (Figura 13), porém há casos em que o exame é negativo e observam-se rupturas pequenas durante a cirurgia.
A ruptura da prótese pode ficar contida dentro da cápsula, chamada ruptura intracapsular, ou pode extravasar pela cápsula, a ruptura extracapsular. No último caso, pode causar mastite induzida pelo silicone e granuloma de corpo estranho.
O tratamento da ruptura consiste na retirada da prótese e da cápsula, idealmente por meio de uma capsulectomia total intacta, para não haver contato do silicone com o tecido mamário.(130)
A ruptura de prótese de mama pode ser clinicamente evidente ao exame físico ou somente identificável por exames de imagem. No exame físico, pode ser identificada perda do formato, da consistência e do volume das próteses, dor, perda da sensibilidade e aumento da dureza nos casos de contratura. A maior parte das rupturas de prótese de mama é diagnosticada somente por exame de imagem.
As causas da ruptura de prótese podem ser iatrogênicas (inadvertidamente durante a cirurgia), tempo da prótese, traumas torácicas, durante mamografia e em contratura capsulares graves.
O principal fator de risco para ruptura é a idade da prótese, tendo uma duração médica entre 12 e 20 anos, seguido de trauma ou defeitos de fabricação. As complicações decorrentes da ruptura podem envolver contratura capsular, migração de silicone para outros tecidos e inflamação local.(129)
Um estudo mostrou que a incidência de ruptura em prótese de mama após 8 anos da cirurgia foi de 12,2% em pacientes submetidas à ressonância nuclear magnética.(131)
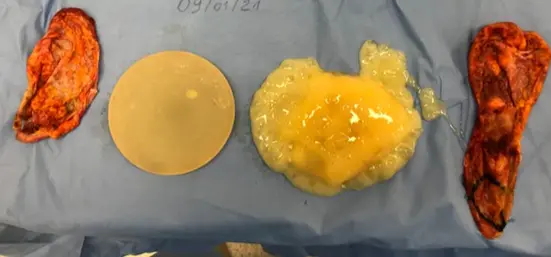
Figura 12. Ruptura de prótese direita com deterioração avançada de seu invólucro. Fonte: Acervo do autor.
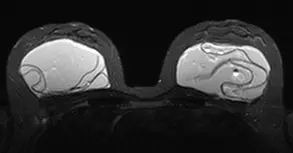
Figura 13. Imagem de ressonância nuclear magnética de próteses de mama rompidas bilateralmente. Fonte: eradiology.com.
Seromas
Os seromas são acúmulo de líquido amarelado e podem ocorrer nas mamas após alguns dias da cirurgia ou de forma tardia, após anos do procedimento (Figura 14). Na maior parte dos casos, o seroma é benigno, não está relacionado com tumores.
Seromas tardios devem ser investigados com exame de imagem como a ressonância nuclear magnética (Figura 15). Guiado pela ultrassonografia, o líquido deve ser aspirado e analisado para descartar BIA-ALCL. Somente 9% dos casos de seroma tardio foram diagnosticados como BIA-ALCL.(132)
Seroma tardio normalmente ocorre pelo descolamento da cápsula de prótese de mama de sua superfície. A presença de seromas espontâneos e de grande volume deve ser investigada pela punção do líquido e análise dele, buscando-se descartar linfoma anaplásico de células grandes. Também foram descritos seromas após infecção por coronavírus, mas a relação precisa ser melhor investigada.(133)
O seroma tardio é raro, com incidência de 1% nas pacientes com prótese de mama. É definido pelo acúmulo de líquido após 12 meses da cirurgia. Normalmente está relacionado a algum trauma leve nas mamas ou infecção subclínica, como biofilme ou micobactéria. Há uma teoria que diz que o seroma tardio é causado pela fricção entre a prótese e a cápsula.(134, 135)
Cápsulas residuais podem secretar líquido, por isso a necessidade de capsulectomia total nos casos de seromas tardios de grande volume e de repetição. Além disso, é necessário a análise de toda a cápsula para excluir BIA-ALCL, nem sempre o diagnóstico é feito somente pelo líquido aspirado.(132, 136
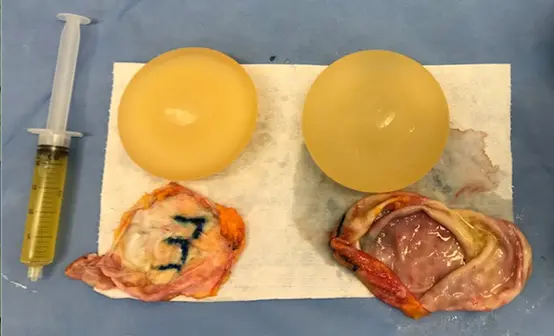
Figura 14. Caso de seroma em prótese de mama esquerda. Fonte: acervo do autor.
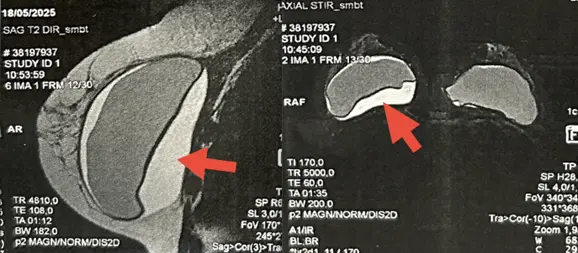
Figura 15. Imagem de ressonância nuclear magnética mostrando seroma (seta vermelha) em prótese de mama. Fonte: acervo do autor.
Dupla cápsula
A primeira descrição da dupla cápsula ocorreu em 2002, em que foi descrita uma cápsula por dentro da outra. Isso ocorre quando a cápsula se solta da superfície da prótese, formando um seroma. À medida que o seroma é absorvido, outra cápsula se forma na superfície da prótese, criando assim duas cápsulas.(137)
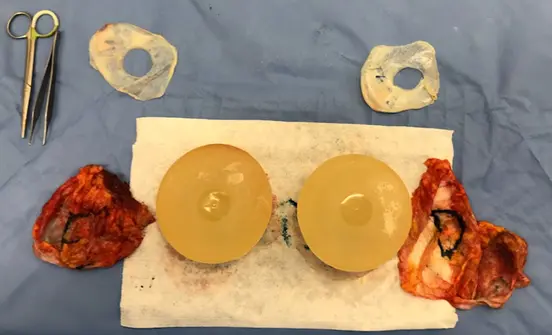
A incidência da dupla cápsula varia entre 2,2 a 8,3% e está mais associada aos implantes de mama macro texturizados, ou seja, mais ásperos.(138) A dupla cápsula pode ser parcial (Figura 16) ou completa, em que se evidencia duas cápsulas envolvendo completamente a prótese. A hipótese da formação da dupla cápsula se dá pela falta da aderência completa entre a prótese e a cápsula.(139, 140)
Outra teoria postula que pequenos traumas descolam a cápsula, formando um espaço onde se acumula seroma. Ocorre principalmente em próteses texturizadas, com superfície áspera.(141)
Deformidade em prótese submuscular
A inclusão de prótese de mama atrás do músculo peitoral maior, conhecido como prótese submuscular ou dual plane, pode causar algumas deformidades no formato. Essas alterações do formato estão associadas somente à prótese submuscular, não estão relacionados à prótese debaixo da glândula ou subglandular.
O tratamento de todas essas deformidades é sempre cirúrgico e pode envolver o reposicionamento da prótese, troca da prótese do plano submuscular para subglandular ou retirada das próteses associada ou não à mastopexia.
Deformidade em dupla bolha (double bubble deformity)
Nesta deformidade (Figura 17) o músculo empurra a prótese abaixo do sulco inframamário, ficando com dois sulcos inframamários. Assim a primeira bolha é da mama que está mais alta e a segunda bolha da prótese que desceu.
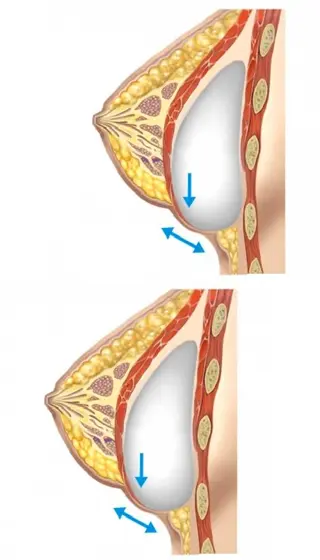
Figura 17. Deformidade em dupla bolha. Fonte: emedicine.com
Deformidade em cascata (waterfall deformity, snoopy nose deformity)
A prótese quando colocada atrás do músculo peitoral maior fica mais fixa e cai menos ao longo dos anos, enquanto a mama pode ceder, principalmente após o emagrecimento ou gestação. Dessa forma a primeira bolha é a prótese mais alta e a segunda bolha é a mama que cedeu. Em inglês essa deformidade também é conhecida como snoopy deformity, em referência ao nariz do cachorro do desenho animado (Figura 18)
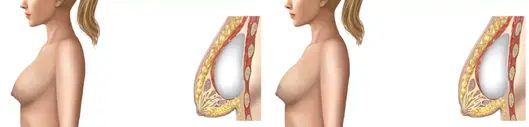
Figura 18. Deformidade em cascata. Fonte: howarthplasticsurgery.com
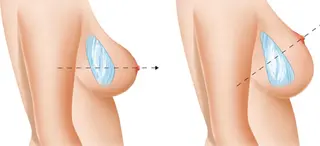
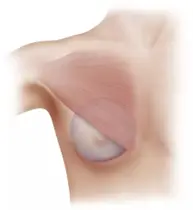
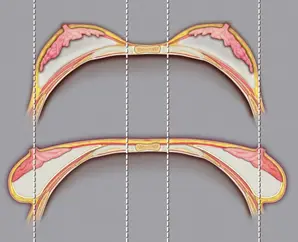

Simastia
GRANULOMA INDUZIDO POR SILICONE (SIG-BIC)
Tem se estudado a reação de corpo estranho (granuloma) induzido pelo silicone que extravasa (gel bleed) pelo invólucro da prótese de mama. Esse extravasamento ocorre devido à alteração da permeabilidade do invólucro da prótese ao longo dos anos. Na Figura 23 é possível observar a coloração amarelada da prótese esquerda rompida em comparação com a prótese íntegra à direita.
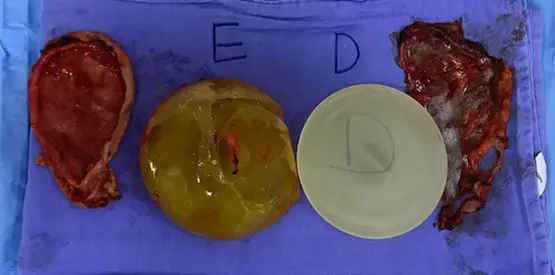
Figura 23. Ruptura e deterioração de prótese esquerda. Fonte: Acervo do autor
A essa condição se deu o nome de granuloma induzido por silicone em cápsula de prótese mamária ou SIG-BIC (Silicone Induced Granuloma in Breast Implan Capsule). Na Figura 24 pode ser observado o aspecto da cápsula com granulomas no seu interior.
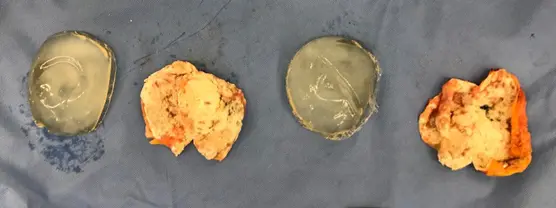
Figura 24. Cápsula mamária com contratura Grau IV, focos de calcificação e de granuloma induzido por silicone. Fonte: Acervo do autor.
O SIG-BIC pode ser um diagnóstico diferencial em relação ao linfoma anaplásico de células grandes, pois possui achados radiológicos parecidos na ressonância nuclear magnética das mamas.
Essa complicação ocorre devido à reação inflamatória desencadeada pelo extravasamento de silicone pelo gel bleed. Esse silicone em contato com a cápsula da prótese de mama desencadeia um processo inflamatório que induz células do sistema imunológico a produzirem tumores/espessamentos na cápsula.(143)
É aventado que o SIG-BIC ou o ALCL são diferentes espectros da mesma doença, ou patologias diferentes que possuem a mesma causa desencadeadora.(144)
Clinicamente, ambas as condições podem se apresentar com aumento do volume mamário às custas de seroma e alterações.
O tratamento da SIGBIC consiste na capsulectomia total intacta, conhecida como explante em bloco. Neste procedimento a cápsula e o granuloma são retirados em conjunto. Não é necessário outro tratamento no pós-operatório.(110, 145)
GRANULOMA INDUZIDO POR SILICONE (SIG-BIC)
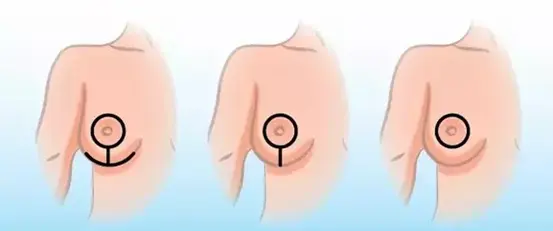
Alternativas de reconstrução da mama após o explante devem ser discutidas entre cirurgião e paciente. A decisão da reconstrução dependerá da queda da mama, chamada de ptose, e do volume que a mama terá ao se retirar a prótese. A queda da mama se baseia na altura da aréola em relação à dobra da mama, chamada sulco mamário. Como demonstrado no Quadro 6 e na Figura 25, pode ser classificada em três graus como leve, moderado e grave.(146)
Quadro 6. Classificação de ptose mamária
Grau de ptose Posição da aréola
II aréola abaixo do sulco mamário
Fonte: Regnault P, 1976.
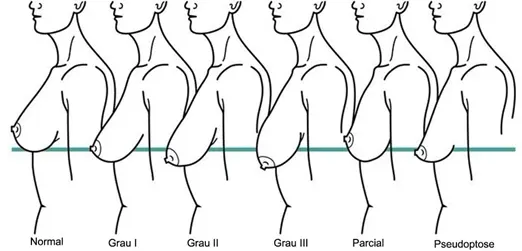
Figura 25. Classificação de ptose mamária. Fonte: enhancemyself.com.
Após o explante, deve ser analisada a necessidade de reconstrução da mama. Pacientes com mamas sem flacidez e volume adequado não necessitam de reconstrução; pacientes com flacidez necessitam de mastopexia (elevação da mama por meio de incisões); e pacientes sem flacidez e pouco volume podem necessitar de enxerto de gordura nas mamas.(147)
Ao longo dos anos em que a paciente teve o implante de silicone, as mamas podem ter tido alguma variação de volume, tanto diminuição por atrofia quanto aumento por ganho de peso.
Em alguns casos de próteses submusculares é necessário fazer a reconstrução do músculo peitoral. Há casos também quando é necessário refazer a dobra debaixo da mama, no jargão médico chamado “sulco inframamário”. Neste caso são realizados pontos cirúrgicos no sulco inframamário para fornecer este suporte, funcionando como um sutiã interno.
Levando em consideração a queda e o volume da mama, as opções cirúrgicas incluem:
• Explante em bloco somente, utilizando a própria incisão prévia. Essa cirurgia é reservada a pacientes com pouca ou nenhuma flacidez nas mamas.
• Explante em bloco mais enxerto de gordura: indicada para pacientes que apresentem gordura suficiente para fazer o enxerto. O enxerto de gordura dará algum volume à mama, mas não o suficiente para se chegar ao volume que se obtém com o uso da prótese. Além disso, parte da gordura é absorvida, podendo ser necessária mais de uma sessão de enxerto de gordura.
• Explante em bloco mais mastopexia com ou sem enxerto de gordura: indicada para pacientes com moderada a grande flacidez mamária. As incisões utilizadas podem ser em torno da aréola, no sulco infra mamário ou a incisão em T invertido, nos casos de maior flacidez (Figura 26). O enxerto de gordura pode ser associado para aumento sutil do volume mamário.(148)
REFERÊNCIAS
1. Goren I, Segal G, Shoenfeld Y. Autoimmune/inflammatory syndrome induced by adjuvant (ASIA) evolution after silicone implants. Who is at risk? Clin Rheumatol. 2015;34(10):1661-6.
2. Colaris MJL, van der Hulst RR, Tervaert JWC. Vitamin D deficiency as a risk factor for the development of autoantibodies in patients with ASIA and silicone breast implants: a cohort study and review of the literature. Clin Rheumatol. 2017;36(5):981-93.
3. Y. S. Video Q&A: what is ASIA? An interview with Yehuda Shoenfeld. BMC Med.2013. p. 118.
4. Y. Shoenfeld NA-L. ASIA – Autoimmune/Inflammatory syndrome induced by adjuvants. Journal of Autoimmunity2011. p. 4-8.
5. Jara LJ, García-Collinot G, Medina G, Cruz-Dominguez MDP, Vera-Lastra O, Carranza-Muleiro RA, et al. Severe manifestations of autoimmune syndrome induced by adjuvants (Shoenfeld’s syndrome). Immunol Res. 2017;65(1):8-16.
6. Perricone C, Alessandri C, Valesini G. [‘ASIA’ – Autoimmune/inflammatory syndrome induced by adjuvants: even and odd]. Reumatismo. 2011;63(2):63-6.
7. BROWN JB, FRYER MP, RANDALL P, LU M. Silicones in plastic surgery; laboratory and clinical investigations, a preliminary report. Plast Reconstr Surg (1946). 1953;12(5):374-6.
8. Brown JB FM, DA O. Study and use of synthetic materials, such as silicones and teflon, as subcutaneous prostheses. . Plast Reconstr Surg1960. p. 264-79.
9. WINER LH, STERNBERG TH, LEHMAN R, ASHLEY FL. TISSUE REACTIONS TO INJECTED SILICONE LIQUIDS. A REPORT OF THREE CASES. Arch Dermatol. 1964;90:588-93.
10. Bridges AJ, Vasey FB. Silicone breast implants. History, safety, and potential complications. Arch Intern Med. 1993;153(23):2638-44.
11. Miyoshi K MT, Kobayashi Y. Hyper-gammaglobulinemia
by prolonged adjuvanticity in men. Disorders developed after augmentation mammaplasty. Jap Med J 1964. p. 9-14.
12. Suh LJ, Khan I, Kelley-Patteson C, Mohan G, Hassanein AH, Sinha M. Breast Implant-Associated Immunological Disorders. J Immunol Res. 2022;2022:8536149.
13. Colaris MJL, de Boer M, van der Hulst RR, Cohen Tervaert JW. Two hundreds cases of ASIA syndrome following silicone implants: a comparative study of 30 years and a review of current literature. Immunol Res. 2017;65(1):120-8.
14. Cohen Tervaert JW. Autoinflammatory/autoimmunity syndrome induced by adjuvants (ASIA; Shoenfeld’s syndrome): A new flame. Autoimmun Rev. 2018;17(12):1259-64.
15. Brawer AE. Mechanisms of Breast Implant Toxicity: Will the Real Ringmaster Please Stand Up. International Annals of Medicine2017.
16. Caldarelli M, Rio P, Giambra V, Gasbarrini A, Gambassi G, Cianci R. ASIA Syndrome: State-of-the-Art and Future Perspectives. Vaccines (Basel). 2024;12(10).
17. Coroneos CJ, Selber JC, Offodile AC, Butler CE, Clemens MW. US FDA Breast Implant Postapproval Studies: Long-term Outcomes in 99,993 Patients. Ann Surg. 2019;269(1):30-6.
18. Ospina-Gómez JE, Ayala-Gutierrez MC, Amaya Muñoz MC, Cáceres Ramírez C, Monsalve-Suárez EF, Saaibi-Solano DL, et al. Adjuvant-Induced Autoimmune Syndrome: A Bibliometric Analysis. Cureus. 2024;16(7):e65184.
19. Gerzenshtein J. The Dishonesty of Referring to Total Intact Capsulectomy as “En Bloc” Resection or Capsulectomy. Plast Reconstr Surg. 2020;145(1):227e-8e.
20. Copeland M, Kressel A, Spiera H, Hermann G, Bleiweiss IJ. Systemic inflammatory disorder related to fibrous breast capsules after silicone implant removal. Plast Reconstr Surg. 1993;92(6):1179-81.
21. de Boer M, Colaris M, van der Hulst RRWJ, Cohen Tervaert JW. Is explantation of silicone breast implants useful in patients with complaints? Immunol Res. 2017;65(1):25-36.
22. Thomas WO, Harper LL, Wong SW, Michalski JP, Harris CN, Moore JT, et al. Explantation of silicone breast implants. Am Surg. 1997;63(5):421-9.
23. Melmed EP. A review of explantation in 240 symptomatic women: a description of explantation and capsulectomy with reconstruction using a periareolar technique. Plast Reconstr Surg. 1998;101(5):1364-73.
24. Jewell ML, Jewell HL. Breast Implant-Associated Illness: Medicine by Belief, So Says Dr. Google. Aesthet Surg J. 2019;39(4):NP87-NP9.
25. Rohrich RJ, Kaplan J, Dayan E. Silicone Implant Illness: Science versus Myth? Plast Reconstr Surg. 2019;144(1):98-109.
26. Disa JJ. Discussion: Silicone Implant Illness: Science versus Myth? Plast Reconstr Surg. 2019;144(1):110-1.
27. Colwell AS, Mehrara B. Discussion: Silicone Implant Illness: Science versus Myth? Plast Reconstr Surg. 2019;144(1):112-3.
28. McCarthy PH, Teitler NA, Hon HH, Miller JJ. Breast Implant Illness and Cutibacterium acnes: A Case Report. Plast Reconstr Surg Glob Open. 2022;10(2):e4146.
29. Slavin SA, Goldwyn RM. Silicone gel implant explantation: reasons, results, and admonitions. Plast Reconstr Surg. 1995;95(1):63-9.
30. Atiyeh B, Emsieh S. Breast Implant Illness (BII): Real Syndrome or a Social Media Phenomenon? A Narrative Review of the Literature. Aesthetic Plast Surg. 2022;46(1):43-57.
31. Manahan MA. Adjunctive Procedures and Informed Consent with Breast Implant Explantation. Plast Reconstr Surg. 2021;147(5S):51S-7S.
32. Magno-Padron DA, Luo J, Jessop TC, Garlick JW, Manum JS, Carter GC, et al. A population-based study of breast implant illness. Arch Plast Surg. 2021;48(4):353- 60.
33. Hoa S, Milord K, Hudson M, Nicolaidis SC, Bourré-Tessier J. Risk of rheumatic disease in breast implant users: a qualitative systematic review. Gland Surg. 2021;10(8):2557-76.
34. Glicksman CA. Commentary on: Understanding Breast Implant Illness. Aesthet Surg J. 2021;41(12):1380-2.
35. Lund H. Commentary on: Understanding Breast Implant Illness. Aesthet Surg J. 2021;41(12):1383-5.
36. Newby JM, Tang S, Faasse K, Sharrock MJ, Adams WP. Commentary on: Understanding Breast Implant Illness. Aesthet Surg J. 2021;41(12):1367-79.
37. Fleury EFC. The contradiction of breast implant illness. Gland Surg. 2021;10(6):2081-3.
38. Yang S, Klietz ML, Harren AK, Wei Q, Hirsch T, Aitzetmüller MM. Understanding Breast Implant Illness: Etiology is the Key. Aesthet Surg J. 2022;42(4):370-7.
39. Ferreira S, Barros AS, Marques M. Breast Implant Illness: Symptoms, Outcomes with Explantation and Potential Etiologies-A Systematic Review and Meta-analysis. Aesthetic Plast Surg. 2025;49(23):6600-20.
40. Spit KA, Azahaf S, de Blok CJM, Nanayakkara PWB. Measuring Platinum Levels in Hair in Women with Silicone Breast Implants and Systemic Symptoms. Plast Reconstr Surg Glob Open. 2022;10(6):e4373.
41. Wixtrom R, Glicksman C, Kadin M, Lawrence M, Haws M, Ferenz S, et al. Heavy Metals in Breast Implant Capsules and Breast Tissue: Findings from the Systemic Symptoms in Women-Biospecimen Analysis Study: Part 2. Aesthet Surg J. 2022;42(9):1067-76.
42. Bresnick SD, Morris S, Lagman C. Findings Consistent with a Breast Implant- associated Somatic System Disorder (BIA-SSD) Among Patients Self-reporting Breast Implant Illness. Plast Reconstr Surg Glob Open. 2024;12(11):e6322.
43. Magnusson MR, McGuire P. Commentary on: Understanding Breast Implant Illness: Etiology is the Key. Aesthet Surg J. 2022;42(4):378-80.
44. Keane G, Chi D, Ha AY, Myckatyn TM. En Bloc Capsulectomy for Breast Implant Illness: A Social Media Phenomenon? Aesthet Surg J. 2021;41(4):448-59.
45. McGuire PA. Commentary On: En Bloc Capsulectomy for Breast Implant Illness: A Social Media Phenomenon? Aesthet Surg J. 2021;41(4):460-2.
46. Steve AK, Temple-Oberle C, Yeung JK, Lafreniere AS, Harrop AR. “You Helped Create This, Help Me Now”: A Qualitative Analysis of Patients’ Concerns about Breast Implants and a Proposed Strategy for Moving Forward. Plast Reconstr Surg. 2021;147(1):16e-24e.
47. Duteille F, Perrot P, Bacheley MH, Bell E, Stewart S. Ten-Year Safety Data for Eurosilicone’s Round and Anatomical Silicone Gel Breast Implants. Aesthet Surg J Open Forum. 2019;1(2):ojz012.
48. Lieffering AS, Hommes JE, van der Hulst R, Rakhorst HA, Verheij RA, Mureau MAM, et al. Breast implant illness revisited: A cohort study of health symptoms in women with implant-based reconstruction. J Plast Reconstr Aesthet Surg. 2025;102:114-22.
49. Hansson SO. The ethics of explantation. BMC Med Ethics. 2021;22(1):121.
50. Suri K, Billick S. Breast Implant Illness Through a Psychiatric Lens. Aesthetic Plast Surg. 2024;48(4):559-67.
51. Bresnick S, Lagman C, Morris S, Robbins M. Correlation Between Medically Diagnosed Anxiety and Depression Disorder and Self-Reported Breast Implant Illness. Aesthet Surg J. 2024;44(10):1118-26.
52. Smith JE, Taritsa IC, Stigliano M, Foppiani J, Lee D, Raska O, et al. Heavy Metals in Breast Implants and Implications for Breast Implant Illness: A Systematic Review of the Literature. Aesthetic Plast Surg. 2025;49(19):5472-9.
53. Wee CE, Younis J, Isbester K, Smith A, Wangler B, Sarode AL, et al. Understanding Breast Implant Illness, Before and After Explantation: A Patient- Reported Outcomes Study. Ann Plast Surg. 2020;85(S1 Suppl 1):S82-S6.
54. Baldwin CM, Kaplan EN. Silicone-induced human adjuvant disease? Ann Plast Surg. 1983;10(4):270-3.
55. Magnusson MR, Cooter RD, Rakhorst H, McGuire PA, Adams WP, Deva AK. Breast Implant Illness: A Way Forward. Plast Reconstr Surg. 2019;143(3S A Review of Breast Implant-Associated Anaplastic Large Cell Lymphoma):74S-81S.
56. Netscher DT. Aesthetic outcome of breast implant removal in 85 consecutive patients. Plast Reconstr Surg. 2004;113(3):1057-9.
57. Swanson E. Evaluating the Necessity of Capsulectomy in Cases of Textured Breast Implant Replacement. Ann Plast Surg. 2020;85(6):691-8.
58. Young VL, Atagi TA, Watson ME. A Prospective Analysis of Patients Undergoing Silicone Breast Implant Explantation. Plast Reconstr Surg. 2000;105(7):2540-3.
59. Fuzzard SK, Teixeira R, Zinn R. A Review of the Literature on the Management of Silicone Implant Incompatibility Syndrome. Aesthetic Plast Surg. 2019;43(5):1145-9.
60. Netscher DT, Sharma S, Thornby J, Peltier M, Lyos A, Fater M, et al. Aesthetic outcome of breast implant removal in 85 consecutive patients. Plast Reconstr Surg. 1997;100(1):206-19.
61. Young VL. Guidelines and indications for breast implant capsulectomy. Plast Reconstr Surg. 1998;102(3):884-91; discussion 92-4.
62. Janowsky EC, Kupper LL, Hulka BS. Meta-analyses of the relation between silicone breast implants and the risk of connective-tissue diseases. N Engl J Med. 2000;342(11):781-90.
63. Bresnick SD. Self-Reported Breast Implant Illness: The Contribution of Systemic Illnesses and Other Factors to Patient Symptoms. Aesthet Surg J Open Forum. 2023;5:ojad030.
64. Wells KE, Roberts C, Daniels SM, Hann D, Clement V, Reintgen D, et al. Comparison of psychological symptoms of women requesting removal of breast implants with those of breast cancer patients and healthy controls. Plast Reconstr Surg. 1997;99(3):680-5.
65. Wells KE, Roberts C, Daniels SM, Kearney RE, Cox CE. Psychological and rheumatic symptoms of women requesting silicone breast implant removal. Ann Plast Surg. 1995;34(6):572-7.
66. Ahern M, Smith M, Chua H, Youssef P. Breast implants and illness: a model of psychological illness. Ann Rheum Dis. 2002;61(7):659.
67. Bresnick SD, Faasse K, McGuire P. The Diagnosis and Management of Patients With Findings Consistent With a Breast Implant Associated-Somatic Symptom Disorder (BIA-SSD). Plast Reconstr Surg Glob Open. 2025;13(5):e6735.
68. McGuire P, Clauw DJ, Hammer J, Haws M, Adams WP. A Practical Guide to Managing Patients With Systemic Symptoms and Breast Implants. Aesthet Surg J. 2022;42(4):397-407.
69. [Available from: www.healingbreastimplantillness.com.
70. www.breastimplantillness.com [Available from: www.breastimplantillness.com.
71. Glicksman C, McGuire P. Commentary on: Self-Reported Health Complaints in Women Undergoing Explantation of Breast Implants. Aesthet Surg J. 2022;42(2):181-2.
72. Miseré RML, van der Hulst RRWJ. Self-Reported Health Complaints in Women Undergoing Explantation of Breast Implants. Aesthet Surg J. 2022;42(2):171-80.
73. Bascone CM, McGraw JR, Couto JA, Sulkar RS, Broach RB, Butler PD, et al. Exploring Factors Associated with Implant Removal Satisfaction in Breast Implant Illness Patients: A PRO BREAST-Q Study. Plast Reconstr Surg Glob Open. 2023;11(9):e5273.
74. Swanson E. Does a Capsulectomy Really Improve Pulmonary Function in Women with Breast Implant Illness? Plast Reconstr Surg Glob Open. 2021;9(11):e3892.
75. Feng LJ, Kumar A. Reply: Does a Capsulectomy Really Improve Pulmonary Function in Women with Breast Implant Illness? Plast Reconstr Surg Glob Open. 2021;9(11):e3902.
76. Food and Drug Administration [Available from: www.fda.gov.
77. Rohrich RJ, Rathakrishnan R, Robinson JB, Griffin JR. Factors predictive of quality of life after silicone-implant explanation. Plast Reconstr Surg. 1999;104(5):1334-7.
78. Rohrich RJ, Bellamy JL, Alleyne B. Assessing Long-Term Outcomes in Breast Implant Illness: The Missing Link? A Systematic Review. Plast Reconstr Surg. 2022;149(4):638e-45e.
79. Bird GR, Niessen FB. The effect of explantation on systemic disease symptoms and quality of life in patients with breast implant illness: a prospective cohort study. Sci Rep. 2022;12(1):21073.
80. Nahabedian MY. The Capsule Question: How Much Should Be Removed with Explantation of a Textured Device? Plast Reconstr Surg. 2021;147(5S):44S-50S.
81. Jewell ML. Commentary on: A Qualitative Study on the Experiences of Women With Breast Implant Illness. Aesthet Surg J. 2022;42(4):394-6.
82. Tang S, Anderson NE, Faasse K, Adams WP, Newby JM. A Qualitative Study on the Experiences of Women With Breast Implant Illness. Aesthet Surg J. 2022;42(4):381-93.
83. Lapid O, Noels EC, Meijer SL. Pathologic Findings in Primary Capsulectomy Specimens: Analysis of 2531 Patients. Aesthet Surg J. 2014;34(5):714-8.
84. Gudjonsdottir LR, Bak EEF, Larsen A, Weltz TK, Ørholt M, Elberg JJ, et al. Is there histological evidence supporting capsulectomy in patients with breast implant illness: A case-control study. J Plast Reconstr Aesthet Surg. 2025;113:138- 46.
85. Al Sammour C, Dziubek M, Danino MA, Ortiz S. Silicone particles in breast implant capsules: A retrospective single-center study evaluating silicone bleeding. Ann Chir Plast Esthet. 2025;70(4):324-34.
86. Lee MA. Reply: Breast Implant Illness, Biofilm, and the Role of Capsulectomy. Plast Reconstr Surg Glob Open. 2020;8(8):e2994.
87. Swanson E. Breast Implant Illness, Biofilm, and the Role of Capsulectomy. Plast Reconstr Surg Glob Open. 2020;8(7):e2999.
88. Magnusson MR. Commentary on: Risk Factors for Explantation of Breast Implants: A Cross-Sectional Study. Aesthet Surg J. 2021;41(8):929-31.
89. Gidengil CA, Predmore Z, Mattke S, van Busum K, Kim B. Breast implant- associated anaplastic large cell lymphoma: a systematic review. Plast Reconstr Surg. 2015;135(3):713-20.
90. Elameen AM, AlMarakby MA, Atta TI, Dahy AA. The Risk of Breast Implant- Associated Anaplastic Large Cell Lymphoma; A Systematic Review and Meta- Analysis. Aesthetic Plast Surg. 2024.
91. Miranda P, Moita F, Vargas Moniz J, Rodrigues Dos Santos C. Breast Implant- Associated Anaplastic Large Cell Lymphoma: Two Distinct Clinical Presentations. Acta Med Port. 2022;35(11):835-9.
92. Bewtra C, Gharde P. Current Understanding of Breast Implant-Associated Anaplastic Large Cell Lymphoma. Cureus. 2022;14(10):e30516.
93. D’Orsi G, Giacalone M, Calicchia A, Gagliano E, Vannucchi L, Vanni G, et al. BIA-ALCL and BIA-SCC: Updates on Clinical Features and Genetic Mutations for Latest Recommendations. Medicina (Kaunas). 2024;60(5).
94. Ward JA, Calderbank T, Tang CC, Goddard NV, MacNeill FA, Tasoulis MK, et al. Estimating the prevalence of Breast Implant Associated Anaplastic Large Cell Lymphoma (BIA-ALCL) – a systematic review. Plast Reconstr Surg. 2024.
95. Azzi AJ, Almadani Y, Davison P. A National Survey to Assess the Population’s Perception of Breast Implant-Associated Anaplastic Large Cell Lymphoma and Breast Implant Illness. Plast Reconstr Surg. 2021;147(4):795-803.
96. Roden AC, Macon WR, Keeney GL, Myers JL, Feldman AL, Dogan A. Seroma- associated primary anaplastic large-cell lymphoma adjacent to breast implants: an indolent T-cell lymphoproliferative disorder. Mod Pathol. 2008;21(4):455-63.
97. Clemens MW, Nava MB, Rocco N, Miranda RN. Understanding rare adverse sequelae of breast implants: anaplastic large-cell lymphoma, late seromas, and double capsules. Gland Surg. 2017;6(2):169-84.
98. Muntean M, Ilies RA, Pop IC, Urian L, Vlad IC, Achimas-Cadariu P. Unveiling the Controversy: A Literature Review on the Link Between Textured Implants and Breast Implant-Associated Anaplastic Large Cell Lymphoma (BIA-ALCL). J Clin Med. 2025;14(11).
99. Clemens MW, Brody GS, Mahabir RC, Miranda RN. How to Diagnose and Treat Breast Implant-Associated Anaplastic Large Cell Lymphoma. Plast Reconstr Surg. 2018;141(4):586e-99e.
100. Shoham G, Haran O, Singolda R, Madah E, Magen A, Golan O, et al. Our Experience in Diagnosing and Treating Breast Implant-Associated Anaplastic Large Cell Lymphoma (BIA-ALCL). J Clin Med. 2024;13(2).
101. Clemens MW, Medeiros LJ, Butler CE, Hunt KK, Fanale MA, Horwitz S, et al. Complete Surgical Excision Is Essential for the Management of Patients With Breast Implant-Associated Anaplastic Large-Cell Lymphoma. J Clin Oncol. 2016;34(2):160-8.
102. Palafox D. Global Adverse Event Reports of Breast Implant-Associated ALCL: An International Review of 40 Government Authority Databases. Plast Reconstr Surg. 2018;141(1):178e-9e.
103. Adrada BE, Miranda RN, Rauch GM, Arribas E, Kanagal-Shamanna R, Clemens MW, et al. Breast implant-associated anaplastic large cell lymphoma: sensitivity, specificity, and findings of imaging studies in 44 patients. Breast Cancer Res Treat. 2014;147(1):1-14.
104. Longo B, Di Napoli A, Curigliano G, Veronesi P, Pileri S, Martelli M, et al. Clinical recommendations for diagnosis and treatment according to current updated knowledge on BIA-ALCL. Breast. 2022;66:332-41.
105. Colwell AS, Lamb LR, Tomczyk E, Faulkner H, Specht MC. An Algorithm for Management of Cosmetic and Reconstructive Patients with Textured Implants: An Institutional Experience. Plast Reconstr Surg. 2021;147(5S):39S-43S.
106. Naga HI, Mellia JA, Basta MN, Morris MP, Christopher AN, Campbell FM, et al. Breast Implant-Associated Anaplastic Large-Cell Lymphoma: Updated Systematic Review and Analysis of Treatment Strategies. Plast Reconstr Surg. 2022;150(4):762-9.
107. Hammond DC. Chronic biofilm infection in breast implants is associated with an increased T-cell lymphocytic infiltrate: implications for breast implant- associated lymphoma. Plast Reconstr Surg. 2015;135(6):1057e-9e.
108. Glasberg SB. Discussion: American Association of Plastic Surgeons Consensus on Breast Implant-Associated Anaplastic Large-Cell Lymphoma. Plast Reconstr Surg. 2024;154(3):486-8.
109. Clemens MW, Myckatyn TM, Di Napoli A, Feldman AL, Jaffe ES, Haymaker CL, et al. American Association of Plastic Surgeons Consensus on Breast Implant- Associated Anaplastic Large-Cell Lymphoma. Plast Reconstr Surg. 2024;154(3):473-83.
110. Kim B, Roth C, Young VL, Chung KC, van Busum K, Schnyer C, et al. Anaplastic large cell lymphoma and breast implants: results from a structured expert consultation process. Plast Reconstr Surg. 2011;128(3):629-39.
111. Talwalkar SS, Miranda RN, Valbuena JR, Routbort MJ, Martin AW, Medeiros LJ. Lymphomas involving the breast: a study of 106 cases comparing localized and disseminated neoplasms. Am J Surg Pathol. 2008;32(9):1299-309.
112. Pro B, Advani R, Brice P, Bartlett NL, Rosenblatt JD, Illidge T, et al. Brentuximab vedotin (SGN-35) in patients with relapsed or refractory systemic anaplastic large-cell lymphoma: results of a phase II study. J Clin Oncol. 2012;30(18):2190-6.
113. Santanelli di Pompeo F, Sorotos M, Clemens MW, Paolini G, Anibaldi P, Davoli M, et al. Mortality Rate in Breast Implant Surgery: Is an Additional Procedure Worthwhile to Mitigate BIA-ALCL Risk? Aesthetic Plast Surg. 2022.
114. Lieffering AS, Hommes JE, Ramerman L, Rakhorst HA, Mureau MAM, Verheij RA, et al. Prevalence of Local Postoperative Complications and Breast Implant Illness in Women With Breast Implants. JAMA Netw Open. 2022;5(10):e2236519.
115. Guimier E, Carson L, David B, Lambert JM, Heery E, Malcolm RK. Pharmacological Approaches for the Prevention of Breast Implant Capsular Contracture. J Surg Res. 2022;280:129-50.
116. Wells HJ, Yang JCC, Edelstein-Keshet L, Isaac KV. Implant Texture and Capsular Contracture: A Review of Cellular and Molecular Pathways. Plast Reconstr Surg Glob Open. 2024;12(5):e5802.
117. Baker JL, Chandler ML, LeVier RR. Occurrence and activity of myofibroblasts in human capsular tissue surrounding mammary implants. Plast Reconstr Surg. 1981;68(6):905-12.
118. Tanna N, Calobrace MB, Clemens MW, Hammond DC, Nahabedian MY, Rohrich RJ, et al. Not All Breast Explants Are Equal: Contemporary Strategies in Breast Explantation Surgery. Plast Reconstr Surg. 2021;147(4):808-18.
119. Montemurro P, Pellegatta T, Pafitanis G. The effect of implant surface on the recurrence rates of capsular contracture following revision breast surgery: Early results from a single surgeon retrospective comparative study. J Plast Reconstr Aesthet Surg. 2021;74(12):3307-15.
120. Knoedler S, Knoedler L, Boroumand S, Alfertshofer M, Diatta F, Sofo G, et al. Surgical Management of Breast Capsular Contracture-A Multi-institutional Data Analysis of Risk Factors for Early Complications. Aesthetic Plast Surg. 2024.
121. Ganon S, Morinet S, Serror K, Mimoun M, Chaouat M, Boccara D. Epidemiology and Prevention of Breast Prosthesis Capsular Contracture Recurrence. Aesthetic Plast Surg. 2021;45(1):15-23.
122. Catic A, Weinzierl A, Heimer J, Pompei B, Harder Y. Smooth Operator: Nanotextured Breast Tissue Expanders Are Associated with Lower Rates of Capsular Contracture. J Clin Med. 2024;13(19).
123. Rotatori DS, Hathaway CL, Steinbach BG, Caffee HH. Noninvasive assessment of implant capsules. Plast Reconstr Surg. 1991;87(4):703-8.
124. Boyd CJ, Chiodo MV, Lisiecki JL, Wagner RD, Rohrich RJ. Systematic Review of Capsular Contracture Management following Breast Augmentation: An Update. Plast Reconstr Surg. 2024;153(2):303e-21e.
125. Bachour Y. Commentary on: Characterizing the Microbiome of the Contracted Breast Capsule Using Next Generation Sequencing. Aesthet Surg J. 2021;41(4):NP150-NP1.
126. Cook J, Pozner JN. Response to “Comments on ‘Characterizing the Microbiome of the Contracted Breast Capsule Using Next Generation Sequencing'”. Aesthet Surg J. 2020;40(9):NP587.
127. Cook J, Holmes CJ, Wixtrom R, Newman MI, Pozner JN. Characterizing the Microbiome of the Contracted Breast Capsule Using Next Generation Sequencing. Aesthet Surg J. 2021;41(4):440-7.
128. Zhang Z, Wang C, Xin M. Comments on “Characterizing the Microbiome of the Contracted Breast Capsule Using Next Generation Sequencing”. Aesthet Surg J. 2020;40(9):NP585-NP6.
129. Szymanski KD, Mikes BA. Breast Implant Rupture. StatPearls. Treasure Island (FL): StatPearls Publishing
Copyright © 2025, StatPearls Publishing LLC.; 2025.
130. Alnaseri T, Musavi L, Deming T, Roostaeian J, Da Lio A, Mason TG, et al. The Surfactant Properties of Clindamycin as a Useful Adjunct for Removing Ruptured Silicone Implants. Plast Reconstr Surg Glob Open. 2024;12(9):e6176.
131. Handel N, Garcia ME, Wixtrom R. Breast implant rupture: causes, incidence, clinical impact, and management. Plast Reconstr Surg. 2013;132(5):1128-37.
132. Honda A, Tsuge I, Kitamura K, Ito H, Yamanaka H, Katsube M, et al. Repeated Fluid Accumulation around a Breast Implant Related to Synovial Metaplasia of the Capsule. Plast Reconstr Surg Glob Open. 2024;12(4):e5759.
133. Chan SLS, Mok JWL. Late Seroma in Breast Implants: A Coronavirus Disease 2019 Phenomenon? Arch Plast Surg. 2022;49(5):611-3.
134. Spear SL, Rottman SJ, Glicksman C, Brown M, Al-Attar A. Late seromas after breast implants: theory and practice. Plast Reconstr Surg. 2012;130(2):423-35.
135. Teitelbaum S. Discussion: late seromas after breast implants: theory and practice. Plast Reconstr Surg. 2012;130(2):439-40.
136. Fosheim K, Bojesen S, Troestrup H, Laenkholm AV. Capsulectomy Can Successfully Treat Chronic Encapsulated Breast Seroma: A Case Report. Cureus. 2022;14(1):e21677.
137. Berry MG, Stanek JJ. The Double Capsule Phenomenon in a Case Series and its Relationship with the Macro-Textured Breast Implant. Aesthetic Plast Surg. 2022:1-6.
138. Berry MG, Stanek JJ. The Double Capsule Phenomenon in a Case Series and its Relationship with the Macro-Textured Breast Implant. Aesthetic Plast Surg. 2023;47(5):1725-30.
139. Danino MA, Giot JP, Efanov JI. Commentary on: Defining Double Capsules: A Clinical and Histological Study. Aesthet Surg J. 2021;41(11):NP1445-NP7.
140. Van Slyke AC, Roller JM, Alaghehbandan R, Carr NJ. Defining Double Capsules: A Clinical and Histological Study. Aesthet Surg J. 2021;41(11):NP1437- NP44.
141. Zogheib S, Hanna C, Daou B, Mjaess G, Nasr M. Breast Implant-associated Double Capsules: What Do We Know So Far? A Systematic Review of the Literature. Aesthetic Plast Surg. 2022;46(1):35-42.
142. Mounir A, Mahdi, S. & Clark, P. Does the reductive mastopexy with implant approach prevent the late bottoming out? : Eur J Plast Surg 2013. p. 757-64.
143. de Faria Castro Fleury E, D’Alessandro GS, Lordelo Wludarski SC. Silicone- Induced Granuloma of Breast Implant Capsule (SIGBIC): Histopathology and Radiological Correlation. J Immunol Res. 2018;2018:6784971.
144. Fleury EF, Rêgo MM, Ramalho LC, Ayres VJ, Seleti RO, Ferreira CA, et al. Silicone-induced granuloma of breast implant capsule (SIGBIC): similarities and differences with anaplastic large cell lymphoma (ALCL) and their differential diagnosis. Breast Cancer (Dove Med Press). 2017;9:133-40.
145. Fleury EFC. Silicone Induced Granuloma of Breast Implant Capsule (SIGBIC) diagnosis: Breast Magnetic Resonance (BMR) sensitivity to detect silicone bleeding. PLoS One. 2020;15(6):e0235050.
146. Regnault P. Breast ptosis. Definition and treatment. Clin Plast Surg. 1976;3(2):193-203.
147. Rohrich RJ, Beran SJ, Restifo RJ, Copit SE. Aesthetic management of the breast following explantation: evaluation and mastopexy options. Plast Reconstr Surg. 1998;101(3):827-37.
148. Mowlavi A, Asghari A, Heydarlou D, Gavilanes E, Sin Z, Mirzania H. Breast Lift Algorithm for the Treatment of Breast Implant Illness Requiring Implant Removal. Aesthetic Plast Surg. 2022.


